真空自耗熔炼钛锭的提纯原理
海绵钛的纯度为99.0%~99.7%,其中杂质约为0.3%~1.0%.杂质可以分为3类:第一类为游离的水、金属镁、MgCl2和TiCl2、TiCl3,它们和钛呈混合物状态夹杂存在;第二类为氧、氮、氢和碳(化合物)等气体杂质,它们在钛中以间隙固溶体形式存在;第三类如铁、硅、锰、钒、钼等金属杂质,在钛中以固溶体的形式存在。
真空自耗电弧熔炼是在真空高温下进行的,每次熔炼都相当于进行一次真空蒸馏和一次区域熔炼,对钛起到一定的精制提纯作用。但这种精制的作用是有限的,区域熔炼的精制作用尤其有限。
1 真空蒸馏的作用
真空蒸馏是利用被蒸馏物中各组分具有不同的挥发性能,对蒸馏物进行低压下加热,通过控制蒸馏温度使一些组分挥发,而与另一些不挥发物达到分离进行提纯的目的。在镁还原生产海绵钛工艺中,对还原物进行真空蒸馏的目的是除去海绵钛中大部分MgCl2和镁,工艺作业制度是一个温度高(1000℃)、中真空和周期长(120~200h)的过程。而真空自耗电弧熔炼这个真空蒸馏过程,与上述过程不同的是,工艺作业制度是温度更高(1800℃)、中真空和周期较短(几小时),它是前者的继续,可以除去海绵钛中残留的杂质,获得纯度更高的金属钛。
真空自耗电弧熔炼按反应器的真空度,可以简化认为蒸发的气体流型属于分子流。与普通蒸馏不同,分子蒸馏仅有被蒸馏物表面的自由蒸发,没有沸腾现象,从理论上说这种自由蒸发是不可逆的。蒸发的气体流型不同,其蒸馏分离系数α也不一样。普通蒸馏分离系数为:![]() 分子蒸馏分离系数为:
分子蒸馏分离系数为:![]()
式中
Pi-i组元蒸气压;
Mi-i组元物质的量;
ri-i组元活度。
钛中各种杂质按其与钛的分子蒸馏分离系数相比,可以分成3种类型:第一种是am>1的杂质,这种杂质可能分离,而且越大越易分离除去,特别是当αm>100时,杂质较易分离除去;第二种是αm=1或接近1的杂质,这种杂质无法除之;第三种是am<1时的杂质,这种杂质在熔炼中无法除去,只能浓缩。
钛和其他一些金属杂质的饱和蒸气压和温度的关系见图1-17和表1-3.一些杂质对钛的分离系数见表1-4.
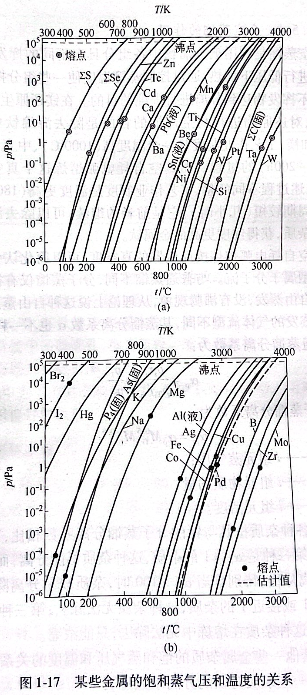
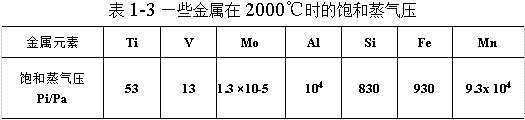
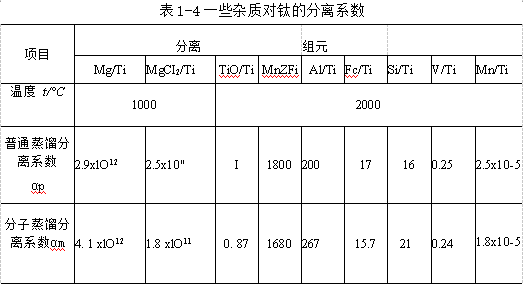
海绵钛中属第一类的游离杂质是容易分离除去的。如Mg和MgCl2挥发性大,也大,500~600℃时开始挥发,到达2000℃时基本上都能除去。又如吸附的水在更低的温度下便开始挥发除去。
海绵钛中夹杂的低价氯化钛,如TiCl2和TiCl3,在一定温度下发生离解反应:
2TiCl2-Ti+TiCl4
4TiCl3-Ti+3TiCl4
生成物中的气态TiCl4被排出炉外。
海绵钛中第二类间隙固溶体杂质氧、氮和碳,它们不能以单元素解析排除,因为钛吸收这些气体杂质后无法解脱。可以认为,它们在钛中以钛化物TiO、TiN、TiC形态存在。而这些钛化物分解压很低,很难离解。如TiN的分解压在2331℃时只有0.31Pa(见表1-5).这些钛化物只能以TiO、TiN和TiC 形态脱除。但是,它们和钛的分离系数为1或接近1,如TiO/Ti的αp为1,无法通过熔炼脱除分离。

钛中的TiO既不能加碳脱氧,也不能加气体CO用还原的方法除氧。因为高温下加碳或加CO均会被钛吸收或分解,相应地会增加钛中的杂质碳和氧。
间隙性杂质氢是唯一能解析脱除的。氢的解析也经过一连串过程,先是氢原子向金属界面扩散,随后在界面上结合成氢分子,氢分子最后在界面脱附,随气流排除。钛含氢浓度低时,生成物为TiH.TiH除氢时,反应历程为:
TiH-Ti+H
2H-H2
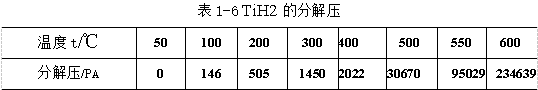
氢化钛的分解压很大(见表1-6),其中的氢很容易被分解脱除。钛锭的最终氢含量可以达到0.002%.
海绵钛中第三类金属杂质,和钛分离系数am>1的有铁、硅等,在熔炼中能挥发除去一些;和钛分离系数am<1的有钒、钼等低挥发性金属,这类杂质在熔炼中只能浓缩,但因含量甚微,不会引起明显变化。
在上述易挥发组分中,H2O、H、TiCl2、TiCl和Ig 最易除去,而MgCl22的比较小且含量多,海绵钛中Cl-含量约为0.05%~0.20%,可以认为它是熔炼中要除去的关键组分,以此来分析除气动力学。
钛真空自耗电弧熔炼时,MgCl2等杂质从液态钛中的挥发,由下述3个步骤组成:
(1)MgCl2从钛液内部通过边界层迁移到熔池表面层;
(2)熔池表面层气相MgCl2脱附和从表面挥发;
(3)气相MgCl2通过气相界面层迁移到气相内部。
不同的杂质元素或化合物的挥发脱除过程,因其挥发性不一样而具有不同的控制步骤。蒸气压较小的杂质Mo、V、TiO、TiN、TiC等,上述第二步骤为其蒸发脱除的控制步骤。蒸气压较大的杂质Mg、MgCl2、H、Mn、Al等,上述第一步骤即边界层传质速度是其蒸发脱除的限制性环节。
在真空条件下,第三步骤的速度很快,不会成为控制步骤,但在氩气氛中熔炼时有可能成为控制步骤。
当MgCl2的表面挥发速度(即第二步骤)成为控制步骤时,有:
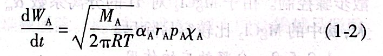
式中
dWA/dt-MgCl2的挥发速度;
αa-MgCl2的凝聚系数;
PAp-纯Mg的饱和蒸气压;
rA-MgCl2的活度系数;
XA-MgCl2在碳中含量(摩尔分数);
M-MgCl2的物质的量。
钛中合金元素的挥发速度也同样可以用式(1-2)进行计算。当控制步骤为第一步骤时,出现表面MgCl2贫化现象,使之产生偏差,此时式(1-2)可写成: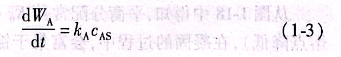
式中
Cas一熔池表面处MgCl2的浓度;
kA-气相表面挥发系数。
液相边界层的传质速度由下式表示:
dMA/dt=Kd(CA-CAs) (1-4)
式中
Ca-熔池内部MgCl2的浓度;
Kd-液相边界层传质系数。
达到稳定时表面挥发速度和界面层传质速度相等,联立式(1-3)和式((1-4),消去CAS值得到: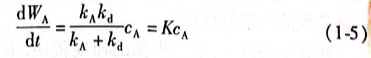
式(1-5)表明,不论挥发过程由气相扩散控制或由液相界面层扩散控制,或者混合控制,挥发速度均和MgCl2浓度成正比,属一级反应。一般情况下,蒸气压大的MgCl2等杂质的蒸发脱除属扩散步骤控制。由于Mgl2对Ti的分离系数am较大,扩散速率也大,钛中的MgCl2比较容易除尽。
2 分凝效应的作用
从前面(第1.2.4节)可知,自耗电弧熔炼时,钛锭的凝固是从锭底部依顺序逐步向上凝固的过程,属顺序凝固。结果,使钛锭的一些合金元素或杂质在整个锭各部位有规律地分布,产生了分凝效应。该效应也是区域熔炼提纯金属的原理。它使钛锭中合金元素或杂质在锭中分布呈现区域偏析。
分凝效应的发生,与钛锭(或金属棒料)中的杂质(或合金元素)的平衡分配常数K.(见式(1-1))有关。现借用一根钛锭自左至右逐步凝固后产生的分凝效应从理论上加以论述,如图1-18所示,就是一根钛锭顺序凝固时锭中杂质的理论分布示意图。而钛锭的实际现状与此相似。
从图1-18中得知,平衡分配常数Ko<1的溶质(它使溶剂的熔点降低),在凝固的过程中,会富集于锭的尾端(右端);与此相
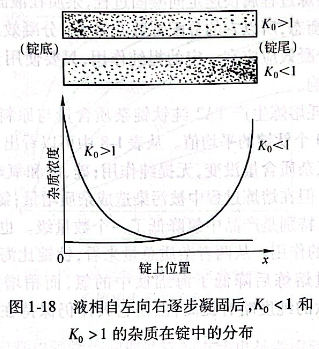
反,Ko>1的溶质(它使溶剂的熔点升高),在凝固的过程中则富集在锭的头部(左端)。接近1的杂质在金属的凝固过程中几乎.y不发生变化,即很难被脱除。越小或K.越大的杂质越易脱除,即提纯效果越好。
实际钛锭中各杂质元素的值见表1-7.
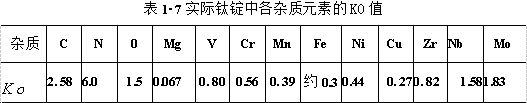
此推断,真空自耗电弧熔炼获得的钛锭,Ko>1的杂质,如碳、氮、氧和铌、钼富集在锭的头部;而Ko<1的杂质,如镁、锰、铬、铁、镍和铜富集在锭尾部的管口处;而接近1的杂质,如钒、锆几乎保持原状,提纯效果差。由此可知,熔铸获得的钛锭,两端富集了一些杂质,在扒皮平头时将锭两端切除,便能保证光锭的质量。
不过,熔炼过程属快速定向凝固过程,杂质在液固两相间扩散无法达到平衡态,所以它的分配常数并非Ko,分凝效应较小一些。
钛熔炼时,分凝效应应有一定的提纯作用,只要使用光锭,便可减少杂质的影响。
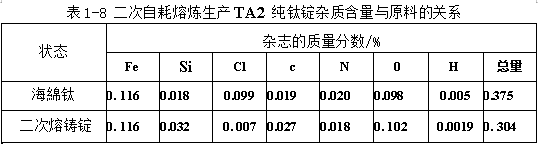
二次自耗熔炼生产TA2纯钛锭杂质含量与原料的关系见表1-8,它是100个钛锭的平均值。从表1-8中可以看出,钛锭和海绵钛中的铁、氮杂质含量没变,无提纯作用;硅、碳和氧略有增加,也无提纯作用,但在熔炼过程中被污染造成杂质增量;氯和氢有明显的提纯效果,特别是产品中氯降低了一个数量级。也说明这主要是真空蒸馏的作用。从两者杂质总量来看,钛锭比海绵钛杂质稍有降低,通过熔炼后降低了海绵钛中的氯,而稍增加了氧等杂质。总之,钛的纯度略有提高,但是它大体仍保持在一个数量级水平。
上一篇:熔炼钛锭凝固时的偏析和收缩
下一篇:真空自耗熔炼过程中钛的损失
 售前咨询专员
售前咨询专员
